新闻及香港科大故事
2026

香港科大故事
团队协作展实力 科大于日内瓦国际发明展勇创历年佳绩
凭借对创新的共同热忱,香港科技大学(科大)及科大(广州)共62支参赛队伍,在3月11日至15日举行的第51届日内瓦「国际发明展」(发明展)中全数获奖,成绩斐然。其中,科大36支队伍与科大(广州)26支队伍合共夺得13项评审团嘉许金奖、20项金奖、20项银奖及9项铜奖。团队的卓越表现更让科大成为本届发明展中囊括最多奖项的香港高等院校。是次佳绩创下历年纪录,不仅彰显了两所院校之间紧密无间的合作精神,更体现了科大不断深化跨境协作、以创新科技推动区域社会与经济发展的坚定承诺。对于这项喜讯,科大副校长(研究及发展)郑光廷教授向各得奖队伍致以热烈祝贺。获奖发明涵盖多个跨学科领域,包括人工智能、医疗健康科技、低空经济及虚拟艺术与平台等。郑教授表示:「展望未来,我们将继续致力营造世界一流的学术与科研环境,鼓励大学社群将科研成果转化为具体可行的解决方案,为社会乃至全人类的长远福祉作出贡献。」今年的发明展吸引了来自全球约40个国家与地区、逾千项发明项目参展。如欲了解更多科大参展发明的详情,请参阅附件。
香港科大故事
科大35周年︰机械光影交织未来新篇
在科大35周年校庆启动礼的璀璨灯光下,舞台上演一幕幕糅合前沿科技的表演,观众见证机械狗运送象征启动时刻的「奇迹球」、人形机械人迎宾致意、无人机于赛马会大堂上空翱翔,生动诠释科大持续探索、勇于创新的精神。这些先进机械人不仅展现科技实力,更诉说着科大人在探索、传承与创业的故事,也正因如此,我们深信凡事可为,奇迹可创活动的一大亮点,是一款配备先进感测技术的机械狗,其感测系统由土木及环境工程学系王幼行教授领导的宏博延展数据研究实验室(Data-Enabled Scalable Research Lab, DESR Lab)研发。王教授现隶属郑家纯机械人研究所(CKSRI),其团队所开发的模块化感测系统,让机械狗能灵活配置不同传感器,以支持多元化的研究及实地应用场景。这款机械狗专为在复杂的户外及工业环境中安全运作而设,并已应用于污水处理设施的建筑检查以及城市树木普查等场景,充分体现了科大致力把前沿科研成果转化为惠及社会的实际应用。活动中亮相的另一款登场可变形模块化的机械狗D1,是全球首款整机模块具身智能机器人,由本末科技研发并捐赠予科大郑家纯机器人研究院。该企业由校友兼科大创始人俱乐部成员张笛创立。D1具备无需对接、突破固化机型限制的模块化设计,可灵活转换为双足、四足、轮足双足及轮足四足等多种形态,构建高度灵活的运动系统,从容应对复杂场景;适用于安防巡检、物资配送及各类高难度任务。其于典礼上的亮相,充分展示科大展现科大在工程创新与创业发展方面相辅相成的独特生态。

香港科大故事
揭开RNA沉默机制的奥秘
Boundless:科大团队在DICER核酸酶上有什么最新发现? 阮教授:我们的研究带来了重大的新发现。DICER是一种在基因沉默中起关键作用的酶,我们发现它其实拥有一种「双口袋」机制,可以精确地量度RNA长度,从而决定切割的位置,犹如一把「精密剪刀」。这个发现颠覆了科学界对DICER如何与RNA链相互作用的传统认知。Boundless:什么是「基因沉默」? 阮教授:基因沉默是指减少或抑制特定基因表现的现象。这个过程可以在细胞内自然发生,也可以通过人工手段诱导实现。基因沉默技术可用于阻止目标基因制造蛋白质,帮助科学家探索基因功能、研究疾病成因,并开发基因治疗方法。Boundless:为什么DICER对基因调控如此重要? 阮教授:DICER在RNA干扰过程中担当重要角色。RNA干扰是细胞利用小型RNA分子来实现基因沉默的一种机制︰DICER负责把长链RNA切割成微小RNA(microRNA),藉此调控基因表现,确保细胞正常运作。Boundless:这次研究的主要突破是什么?阮教授:我们首次发现了DICER中有一个「偏好辨识尿嘧啶结合口袋」(G-favored binding pocket),能够识别以鸟嘌呤开头的RNA链。在此之前,科学界以为DICER只有一种排斥鸟嘌呤的口袋。我们的新发现改写了这个观念,为DICER的运作机制提供了全新视角。Boundless:研究团队使用了哪些研究方法? 阮教授:我们结合了大数据分析与高分辨率成像技术,通过大量切割实验,观察了数千种RNA变体与DICER互动的情形,并利用低温电子显微镜(Cryo-EM)技术,在原子级别上清楚呈现DICER与RNA结合的过程。Boundless:研究过程中遇到了哪些挑战?

新闻
科大研究团队开创有机催化创新策略 合成具有抗病毒潜力的手性亚磺酰胺
由香港科技大学(科大)化学系讲座教授及国家人体组织功能重建工程技术研究中心(香港分中心)主任孙建伟教授领导的研究团队,近日在有机合成与药物化学领域取得突破性进展——研发出一种基于空气稳定型手性膦催化剂的对映选择性合成方法,成功制备出高对映体纯度的 S(IV)手性乙烯基亚磺酰胺。这类有机硫化合物此前研究较少,却展现出良好的抗病毒应用潜力。手性硫中心化合物在药物研发与有机合成中的重要性毋庸置疑。在市面上畅销的小分子药物中,超过四分之一含有硫原子;而具有S(IV)手性的手性亚磺酰胺,更是药物化学、不对称合成助剂及催化配体领域的关键合成砌块。然而,目前制备高对映体纯度亚磺酰胺的方法均依赖过渡金属催化,并需使用有机金属亲核试剂,高效的有机催化策略长期处于空白状态,成为这一高价值化学领域的关键短板。为解决这一难题,孙建伟教授团队在《自然・化学》发表标志性研究成果,详细阐述了一款基于 SPHENOL 手性骨架设计合成的新型 C₂对称手性膦催化剂——QianPhos。该催化剂兼具优异的空气稳定性与结构刚性,可催化森田-贝利斯-希尔曼(MBH)酯与亚磺酰胺之间发生 [3+2] 环加成反应,实现高化学选择性、高对映选择性与高非对映选择性的碳 - 硫键构建。与传统过渡金属催化方法不同,该有机催化策略通过原位生成磷叶立德作为乙烯基亲核试剂,为制备高对映体纯度的手性环状乙烯基亚磺酰胺提供了一条机理独特的新路径。这类环状乙烯基亚磺酰胺能与新冠病毒突变刺突蛋白(SARS-CoV-2)及人类免疫缺陷病毒1型(HIV-1)的 ENV 蛋白高效结合,凸显出这一尚未被充分探索的化学领域在抗病毒药物研发中的巨大潜力。团队结合密度泛函理论(DFT)计算与核磁共振(³¹P、¹⁹F NMR)机理实验,揭示了该反应的核心机理特征:膦鎓物种为催化剂的休眠态,而亚磺酰胺则兼具双重作用——既是反应底物,又可作为促进剂推动关键催化中间体膦鎓的形成。这一尚未见报道的机理特征,正是该反应具备高选择性的核心原因。
新闻
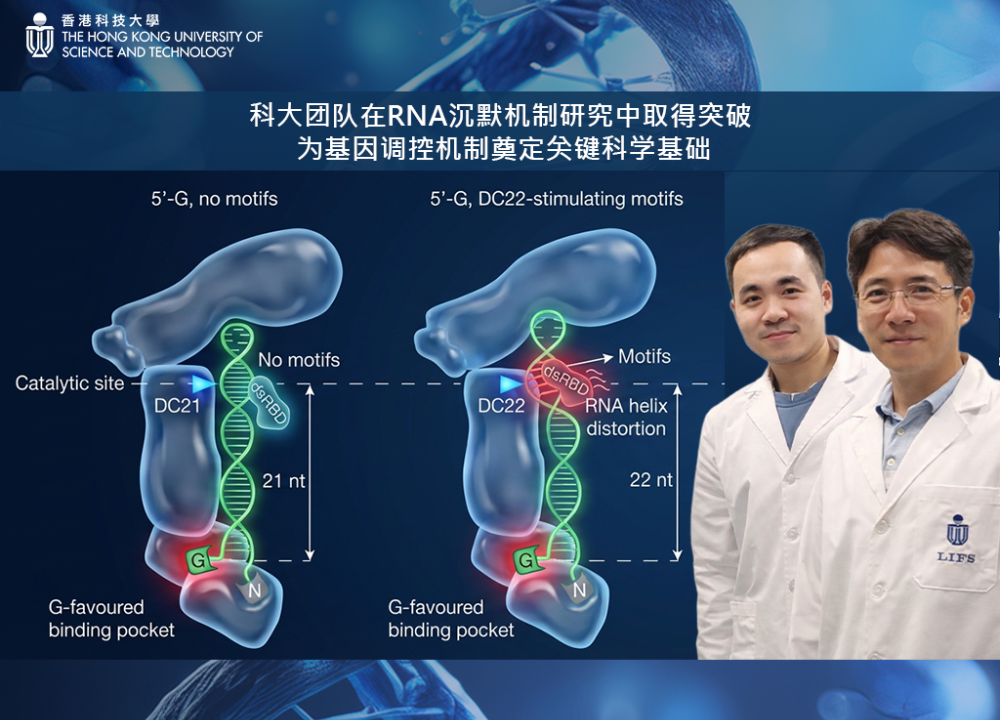
科大团队在RNA沉默机制研究中取得突破
香港科技大学(科大)研究团队在生物学 RNA 沉默机制研究中取得突破性发现,发现人类体内关键核酸酶DICER能精准调控微小核糖核酸(microRNAs, miRNA)的机理。这一科研突破将有助推动基因调控研究的发展,为深入了解癌症、免疫系统疾病及遗传疾病机制提供全新角度。这项研究由科大生命科学部副教授阮俊英教授(Tuan Anh NGUYEN)领导,并由博士生Minh Khoa NGO与Cong Truc LE共同完成,并以《DICER cleavage fidelity is governed by 5′-end binding pockets》为题撰写论文刊登于国际级学术期刊Nature。人类生命的讯息由DNA基因组负责编码,并透过信使RNA(核醣核酸)传递与执行 DNA的遗传讯息。RNA通常是单股,由核醣与 A(腺嘌呤)、U(尿嘧啶)、G(鸟嘌呤)、C(胞嘧啶)四种核糖核苷酸组成。RNA参与许多细胞的重要功能,包括製造蛋白质、调控基因表现,甚至在某些病毒中充当遗传物质。在RNA的世界中,DICER 核酸酶扮演关键的「精密剪刀」角色,它会将双股RNA切割成极短的小片段,使这些小RNA能进入细胞的沉默系统,用来辨识并关闭错误或不需要的基因讯息,犹如在文章中标记与删除错字。

新闻
科大开发全球首个材料AI工具GrainBot 开辟微结构量化分析新途径
香港科技大学(科大)研究团队成功开发人工智能(AI)工具GrainBot,能从显微图像中自动提取并量化多种材料的微结构特征。GrainBot旨在应对材料科学领域对数据驱动及自主研究流程日益增长的需求,提供系统化的方法将复杂图像信息转化为可量化数据,从而加速新一代材料的研发进程。微结构的定量分析一直是材料科学多个领域的关键难题。尽管先进显微技术能够获取高质量的材料图像,但其中蕴含的信息往往难以通过可靠且高效的方式进行分析。现有方法多聚焦于识别简单特征或进行图像分类,难以揭示不同微结构参数之间的互动关系,阻碍了研究人员深入理解材料结构与性能的关联,减缓新材料的设计与优化。为突破此瓶颈,由科大化学及生物工程学系副教授周圆圆教授领导的团队设计出GrainBot,为分割、特征测量和结构相关性分析提供一体化解决方案。研究团队利用卷积神经网络实现精确的晶粒分割,并结合自研算法测量晶粒面积、晶界沟槽以及表面起伏凹陷等特征。GrainBot能将显微图像转化为多维度的丰富数值指标,有助研究人员建立大型及标准化微结构数据库,摆脱仅依赖定性观察的限制。研究团队将GrainBot应用于一款高效太阳能电池关键材料——金属卤化物钙钛矿薄膜,以验证工具的效能。透过分析不同底部表面形貌样本的原子力显微镜图像,GrainBot成功建构涵盖数千颗独立晶粒的数据库,每颗晶粒均标注多项微结构参数。配合统计分析,便能找出晶粒普遍分布的规律,以及不同特征之间过往难以量化的关系,例如晶粒尺寸、沟槽几何形状与表面粗糙度等的隐藏关联性。除分析统计外,研究更结合可解释的机器学习模型,以揭示微结构特征的相互影响机制。团队以选定的晶粒测量参数为目标,训练基于梯度提升的决策模型,并运用特征重要性分析与特征影响关系图等解析工具,探讨晶粒表面积与晶界沟槽等参数如何共同影响表面凹深或凸脊高度。
新闻
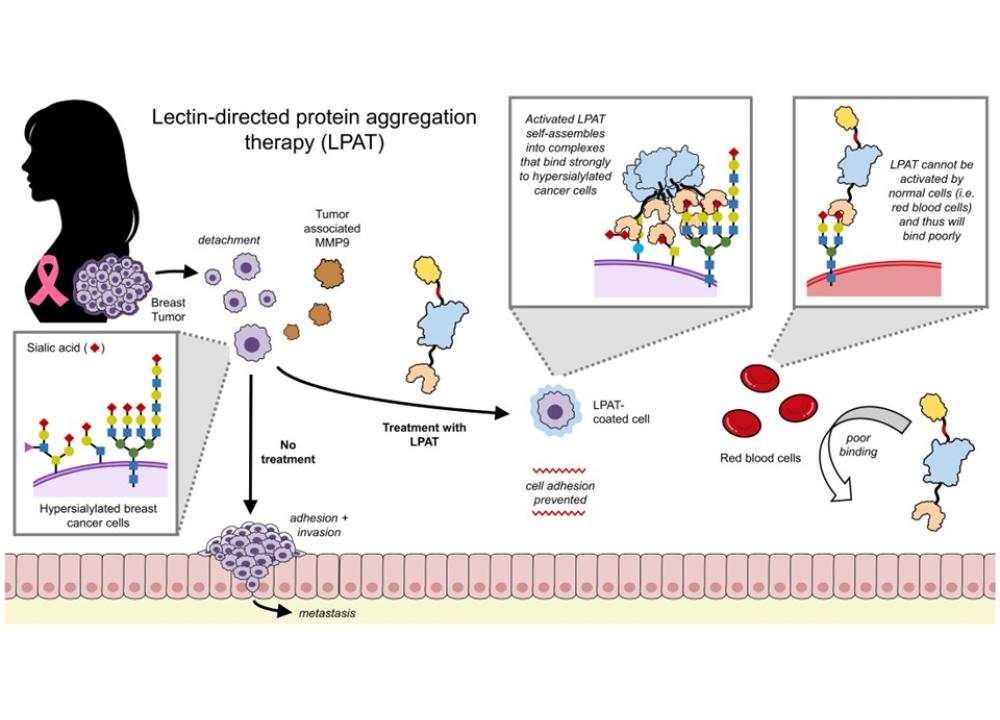
科大研究团队研发创新聚糖靶向系统 有助开发转移性肿瘤预防疗法
香港科技大学(科大)化学系助理教授黄敬皓教授领导的研究团队近日透过生物工程技术取得重大突破,研发出新型的聚糖靶向系统,称为「凝集素定向蛋白聚集疗法(LPAT)」。透过这项技术,研究团队成功在小鼠模型中开发出能够预防转移性乳腺癌形成及生长的治疗方法。靶向抗癌疗法具有难以替代的临床价值,其通过更严格筛选、更精准的方式消除癌细胞,可避免传统化疗常有的严重副作用。现时,癌症靶向疗法主要採用单克隆抗体技术,该技术通常被设计用于识别癌细胞表面过度表达的特定生物标志物。尽管抗体在靶向治疗领域的影响无可比拟,但其亦存在一项众所周知的局限——无法有效区分癌细胞相关的聚糖与正常健康组织中的聚糖。因此,众多靶向聚糖的抗体药物均未能通过临床试验。许多癌组织在生长和转移至身体其他部位时,其细胞表面聚糖水平会显著升高,然而目前针对该靶点的有效干预策略仍属空白,未能充分实现靶向糖基化治疗的潜力。为攻克此难题,黄教授的研究团队近期于《Biomaterials》期刊发表一项研究,提出一种新策略:透过生物工程设计的蛋白质疗法,选择性地结合富含唾液酸(即高唾液酸化)的乳腺癌细胞。该治疗剂利用高转移性癌细胞分泌的天然蛋白酶释放活化蛋白,随后该活化蛋白可自组成六聚体蛋白复合物,从而强力结合高唾液酸化乳腺癌细胞。反之,当遇到正常细胞如红血细胞时,治疗剂因无法满足激活条件而结合能力极弱。研究显示,该技术能显著抑制高转移性乳腺癌细胞的黏附、侵袭及迁移活性。此外,研究团队还证明该疗法能完全抑制转移性肺肿瘤在小鼠体内形成。回顾这项成果,黄教授表示:「我们在这项研究中观察到的聚糖识别精度,是抗体技术难以轻易实现的。鉴于目前仅触及该技术的表层,我们非常期待进一步探索转移预防疗法的可能性。」
新闻
科大研究发现以污水系统处理湿厨余成本效益更高
香港科技大学(科大)研究团队透过分析香港、北京、纽约等全球29个大城市的厨余数据,建立了一套创新的城市厨余管理框架。研究指出,在厨余含水量较高的「湿厨余城市」如香港,将厨余搅碎并导入污水系统进行处理,比单靠依靠堆填更具效益,此举更可令整体温室气体排放量降低约 47%,同时减少约 11%的废物处理成本。该研究为全球城市的厨余管理提供全新的量化依据。研究由科大土木及环境工程学系讲座教授陈光浩教授领导,团队成员包括博士后研究员郭洪骁博士及博士生邹旭等,并与华中科技大学研究团队合作。研究成果以〈Redefining separate or integrated food waste and wastewater streams for 29 large cities〉为题,在国际学术期刊《Nature Cities》上发表。随着全球都市人口上升,厨余量亦不断增加。目前,大部分城市仍採用堆填或焚化的方式处理厨余,然而高含水量的厨余显着增加运输成本及能源消耗。例如在美国,堆填区中的厨余产生的甲烷佔整体堆填区排放量的58%,已成为主要的温室气体污染来源之一。研究团队通过收集全球29个大城市的厨余组成、污水量、能源消耗与处理成本等数据进行科学分析,发现影响厨余处理效益的关键因素并非厨余重量及种类,而是其含水量(moisture load)。含水量愈高,固体废物处理系统的负荷愈大,相应的处理成本和排放量也会随之增加。研究团队提出的「城市生物废弃物通量」(Urban Biowaste Flux, UBF)框架计算出,当城市每年人均厨余含水量达到46.8公斤时,採用透过污水系统结合堆填或焚化的「整合方式」处理厨余,会比单纯以固体废物方式处理更加有效。香港、北京及首尔等汤水及新鲜食品比例较高的城市均属于典型的湿厨余城市。研究显示,在这类城市中,使用厨余研磨器把厨余导入污水系统,有助提升整体处理效能。以香港为例:








