新闻及香港科大故事
2026
新闻
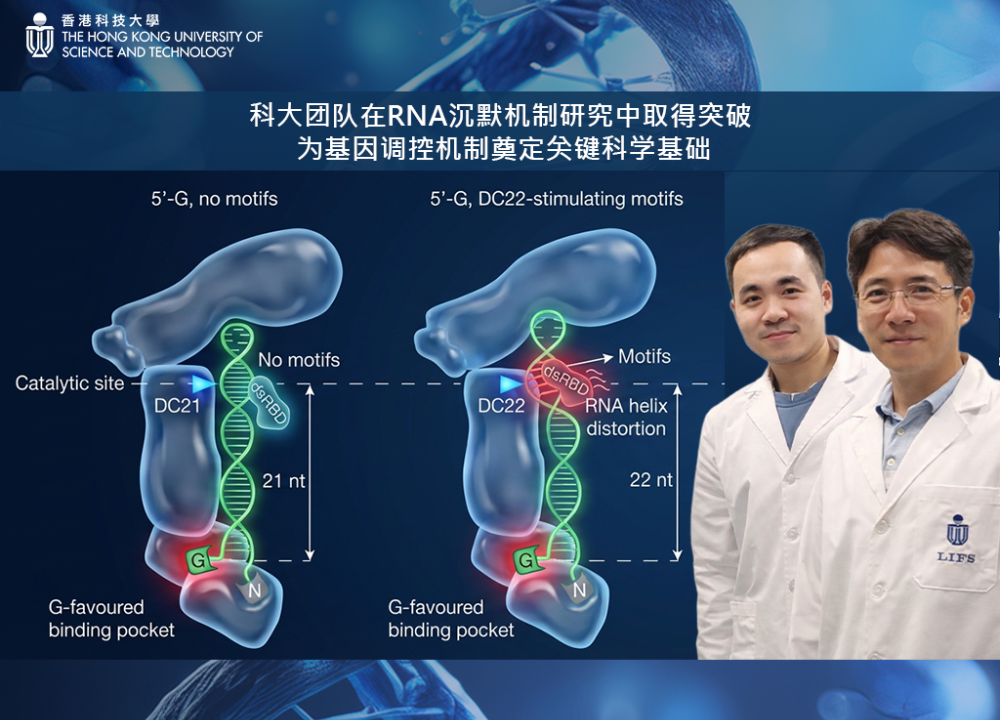
科大团队在RNA沉默机制研究中取得突破
香港科技大学(科大)研究团队在生物学 RNA 沉默机制研究中取得突破性发现,发现人类体内关键核酸酶DICER能精准调控微小核糖核酸(microRNAs, miRNA)的机理。这一科研突破将有助推动基因调控研究的发展,为深入了解癌症、免疫系统疾病及遗传疾病机制提供全新角度。这项研究由科大生命科学部副教授阮俊英教授(Tuan Anh NGUYEN)领导,并由博士生Minh Khoa NGO与Cong Truc LE共同完成,并以《DICER cleavage fidelity is governed by 5′-end binding pockets》为题撰写论文刊登于国际级学术期刊Nature。人类生命的讯息由DNA基因组负责编码,并透过信使RNA(核醣核酸)传递与执行 DNA的遗传讯息。RNA通常是单股,由核醣与 A(腺嘌呤)、U(尿嘧啶)、G(鸟嘌呤)、C(胞嘧啶)四种核糖核苷酸组成。RNA参与许多细胞的重要功能,包括製造蛋白质、调控基因表现,甚至在某些病毒中充当遗传物质。在RNA的世界中,DICER 核酸酶扮演关键的「精密剪刀」角色,它会将双股RNA切割成极短的小片段,使这些小RNA能进入细胞的沉默系统,用来辨识并关闭错误或不需要的基因讯息,犹如在文章中标记与删除错字。
2025

新闻
诺贝尔奖得主汇聚科大:以好奇心为舟 航向科学卓越之境
香港科技大学(科大)近日邀得三名诺贝尔奖得主,与近200名师生和嘉宾作现场交流。 活动同时吸引了约2,000名来自内地各个高等院校的线上观众参与,彰显科大在推动跨学科创新,以及连结本地科研社群与全球思想领袖方面的努力。
作为今年「香港世界青年科学大会」暨「香江诺贝论坛」的主题活动,这场名为「我与科学家在一起:诺贝尔奖得主走进科大」的活动于4月14日举行,由科大与香港北京高校校友联盟(京校联) 合办。 三位享誉国际的诺贝尔奖得主分享了他们的真知灼见:
May-Britt MOSER教授:2014年诺贝尔生理与医学奖得主,以发现大脑空间导航系统中的网格细胞闻名
Konstantin NOVOSELOV教授: 2010年诺贝尔物理学奖得主,因石墨烯和二维材料的卓越研究获奖
Didier QUELOZ教授:2019年诺贝尔物理学奖得主,因首次发现一颗围绕类太阳恒星的系外行星而改写了天文学史
这三位顶尖科学家分享了他们的科研历程以及对未来科学突破的展望,同时强调好奇心驱动研究的重要性。
科大校长叶玉如教授感谢一众贵宾亲临校园,并衷心答谢主办方和支持机构的精心安排。 她说:「今天的活动不仅让师生有机会与优秀的科学家交流,更能一同深入探索科学研究的本质。 科大自创校以来,一直秉持推动创新、研究与知识转移的使命,而这些诺贝尔奖得主所展现的好奇心、创造力与坚毅不屈的精神,正正是科大致力培养学生所具备的素质。 我期盼他们的科研历程,能启发师生们继续追求突破,透过跨学科、跨地域的合作,共同发掘知识的力量,造福社会。」

新闻
科大生命科学团队建立颅内视束损伤模型 揭示重塑中枢神经系统损伤后功能性环路的关键机制
由香港科技大学(科大)生命科学部和化学及生物工程学系刘凯教授领导的研究团队,成功开发了一种颅内橄榄顶盖前核(OPN)前视神经束损伤模型(pre-OPN OTI),并揭示了重塑受损中枢神经系统功能性环路的关键机制,为神经创伤以及神经退行性疾病的精准治疗提供了崭新方向。
成年哺乳动物的中枢神经系统(CNS)一旦损伤,其自我修复能力较低,主要原因在于损伤后神经轴突无法再生,亦无法与目标神经元重建功能性连接。目前的研究多聚焦在增强轴突再生能力,但仅有少数模型能在完全性损伤后实现功能性连接,而且重建功能性连接机制仍不明确。为此,刘凯教授的团队展开相关研究,成功开发了颅内橄榄顶盖前核前视神经束损伤模型,该研究结果于2025年3月在《Nature Communications》上发表,题为「Functional optic tract rewiring via subtype- and target-specific axonal regeneration and presynaptic activity enhancement」。
该模型通过显微手术在小鼠外侧膝状体(LGN)与OPN间施加机械压力,精确地使小鼠视网膜神经节细胞(RGCs)轴突受到损伤。相较于传统模型,该模型有几个显著优势──无需移除皮层组织,手术时间缩短;损伤位点距离靶核团OPN接近,便于研究靶向轴突再生;利用瞳孔光反射(PLR)作为功能恢复指标,实现定量评估;RGCs存活率高,可作长期观察。研究透过完全丧失PLR以证实损伤的完整性(因PLR由内在光敏视网膜神经节细胞ipRGCs经OPN环路介导),并通过瞳孔收缩定量监测功能恢复进程。
2024

新闻
科大举办「分子前沿研讨会」 汇聚四名诺贝尔奖得主 激发年轻一代科创热情
香港科技大学(科大)今天起一连三日于大学的逸夫演艺中心举办「分子前沿研讨会」(Molecular Frontiers Symposium),邀得多位国际知名科学家,包括四名诺贝尔奖得主出席演讲,为一众顶尖学者及年轻新一代,提供多元化思想领袖平台,促进交流与联系。
来自世界各地近40名国际顶尖分子科学家,包括诺贝尔奖得主斯特凡‧赫尔(Stefan HELL) 教授、蒂姆‧亨特(Tim HUNT) 爵士、卡尔‧巴里‧夏普利斯(K. Barry SHARPLESS) 教授和格雷戈里‧温特(Gregory WINTER) 爵士,将于大中华区首届题为「科学新知的前沿」的研讨会上,就基因编辑、萤光显微镜及蛋白质工程等议题,分享真知灼见及相关领域的最新发展。
研讨会录得逾1,500名报名参与嘉宾,当中包括数百名来自香港和其他大湾区城市的学生,以及生物科技与生物医学范畴的专家和业界代表等。在研讨会的答问环节上,与会同学向现场的顶尖讲者踊跃提问,了解他们于研究路上所面对的得与失。各讲者分享他们的独到见解和心得,为有志投身科研创新的学生带来启发。
活动主办方分子前沿基金会(Molecular Frontiers Foundation)创会主席Bengt NORDEN 教授表示:「分子前沿研讨会旨在激发下一代对科学的热情,推动分子科学的创新研究,并促进顶尖科学家与大众之间具意义的互动。我们很高兴是次盛会首次在香港举行。香港是一个充满活力的国际教育枢纽,拥有五所位列全球百强的大学,而科大是当中一所致力于创新与研究的大学。透过于科大汇聚这批卓越的学者,我期望能激发富有成果的讨论并促进跨地域合作,从而帮助塑造分子科学的未来。」

新闻
科大团队发现新的细胞因子促进SARS-CoV-2进入宿主细胞
由香港科技大学(科大)生命科学部副教授郭玉松教授带领的研究团队,最近揭示了一项有关新型冠状病毒(SARS-CoV-2)的新发现。团队最新发现的宿主因子会通过与SARS-CoV-2刺突蛋白的受体结合域相互作用,来促进病毒进入细胞。这项发现不但为我们理解SARS-CoV-2感染机制带来新视角,更为治疗新冠提供了新方向。
科学界普遍认为,SARS-CoV-2的侵染过程主要依赖其刺突蛋白的受体结合域(CoV2-RBD)与宿主细胞受体ACE2的相互作用。过往虽然有大量研究围绕ACE2的过度表达如何促进病毒入侵宿主细胞,但对于缺乏ACE2是否能抑制病毒入侵的探究却相对较少。就此,由郭玉松副教授带领的科大团队,遂与香港大学(港大)和香港理工大学(理大)的研究团队,展开联合研究,透过GST pull-down方法,成功筛选出除了ACE2之外、与CoV2- RBD结合的多种宿主表面因子。
实验结果显示,在经筛选的众多宿主表面因子中,宿主因子SH3BP4调节了CoV2-RBD的内吞过程,并以不依赖ACE2,而是依赖整合素和网格蛋白的方式,介导SARS-CoV -2伪病毒进入宿主细胞。这项发现揭示了SH3BP4在病毒透过内吞途径入侵宿主过程中扮演的重要角色。除了SH3BP4外,部份经筛选的细胞因子,例如ADAM9和TMEM2,相比于感染力相对低的SARS-CoV的RBD,对CoV2-RBD显示出更强的亲和力,表明这些因子于SARS-CoV- 2入侵中具有特定作用。此外,研究团队更发现了偏好与SARS-CoV-2 Delta变异株的RBD结合的因子,有可能进一步增强Delta变异株的入侵能力。
郭玉松教授表示:「本次研究不仅揭示了SARS-CoV-2入侵宿主细胞过程中发挥作用的新宿主细胞表面因子,还发现了整合素在介导病毒内吞中的关键作用,为治疗新冠奠下新的研究基础。」
2023

新闻
科大研究揭示IGF2分泌通路如何调控肌肉干细胞分化机制 为治疗多种疾病提供理论基础
由香港科技大学(科大)领导的研究团队,近日揭示类胰岛素生长因子2 (IGF2) 如何调控肌肉干细胞分化,这对通过抑制IGF2分泌以操控其讯号路径的潜在治疗策略提供理论基础。
IGF2在细胞增殖、迁移、分化和存活等过程中起着关键作用。 它的功能失调会导致多种生长障碍,包括银罗素综合症 (Silver–Russell syndrome) 和贝克威思–威德曼症候群 (Beckwith–Wiedemann syndrome)。 虽然IGF2的表达和其激活的下游讯号传导途径已被广泛研究,但新合成的IGF2蛋白如何高效地分泌以发挥其功能仍然未明。
近日,由科大生命科学部副教授郭玉松所领导的团队发现,新合成的IGF2需要经过几个细胞内转运站,包括内质网和高尔基体,才能被细胞分泌出来。 团队发现一种名为TMED10的I型跨膜蛋白,能够识别IGF2上的转运信号,从而促进IGF2从内质网到高尔基体的运输。 团队进一步研究发现,这种调控是TMED10的GOLD结构域与IGF2的112-140残基直接相互作用的结果。 此外,质谱分析显示TMED10也介导了单通道跨膜蛋白sortilin的内质网输出。 后续研究表明,sortilin有助于IGF2的高尔基体后转运,这意味着TMED10间接地介导了IGF2从高尔基上的输出。 研究团队也在小鼠的C2C12肌母细胞中验证了他们的模型,证明TMED10调节了C2C12细胞中IGF2的分泌,进而调控肌肉干细胞分化。
郭教授说:「这些发现增进了我们对IGF2的生理作用、疾病机制和潜在治疗应用的理解。 在特定条件下,IGF2信号通路的过度激发会触发不受控的细胞增长,或会导致癌症。 透过调控IGF2细胞内转运过程,我们或能调节IGF2信号通路以达到临床治疗效果。 此外,由于IGF2在组织修复和再生中发挥关键作用,因此通过在体内过度表达其货物受体来增强其释放,可能有助于加速伤口愈合。 」

新闻
科大研究团队研发创新显微镜平台 揭示骨骼肌再生中的复杂动态过程
香港科技大学(科大)的研究团队开发出一个由双镭射非线性光学显微镜构成的先进平台,以研究肌卫星细胞在肌肉再生过程中的动态。透过这项突破性技术,团队发现了肌卫星细胞在肌肉修复中的新行为机制,有助进一步推动研发针对肌肉相关疾病的标靶治疗策略。
骨骼肌的再生过程依赖肌卫星细胞与各种细胞成分之间的复杂协作。当肌肉受伤时,随着肌卫星细胞的激活,髓系细胞会迁移到伤口处。以往有研究已发现在肌肉微环境中静止肌卫星细胞的形态异质性,这些细胞透过建立特异的细胞黏附和空间排列,以维持其静止状态。然而,由于缺乏适合的活体动物成像技术,研究人员难以分析肌卫星细胞与髓系细胞之间的相互作用。
近日,科大电子及计算机工程学系教授瞿佳男的团队开展跨学科合作,研发出一个双镭射多模式非线性光学显微镜平台,可对活体骨骼肌中各种细胞类型和结构进行高解析度成像,并由科大生命科学部教授邬振国的团队提供肌肉生物学和再生过程方面的专业知识。利用这项创新成像技术,他们的联合研究为控制肌肉再生的复杂过程提出新见解。当中有趣的是,这项研究颠覆了普遍认为非肌源性细胞是激活肌卫星细胞的主要驱动因素的想法。团队发现肌卫星细胞具备一种内在能力,可以在不依赖非肌源性细胞外部信号的情况下,感知和回应再生信号。
研究亦分析了髓系细胞,尤其是巨噬细胞,在调节肌卫星细胞行为中的作用。团队发现巨噬细胞对肌卫星细胞的激活并非必需,不过在肌肉再生过程中,巨噬细胞为肌卫星细胞的增殖和分化发挥关键作用。巨噬细胞的减少导致再生过程中肌卫星细胞分裂受损和肌肉纤维化增加,显示它们在促进有效肌肉再生方面具有阶段依赖性的作用。
此外,研究探讨了非肌源性细胞与肌卫星细胞之间的即时相互作用。这两种细胞类型之间的持续物理接触对于肌卫星细胞的激活或细胞分裂并非必要,反而是非肌肉细胞的旁分泌信号似乎能调节肌卫星细胞的增殖,这反映了非肌肉细胞分泌因子在协调肌卫星细胞再生过程中的重要作用。
瞿教授表示:「利用先进的成像技术,这项研究为肌肉再生中复杂的细胞相互作用提供了全面的学术探讨,揭示肌卫星细胞行为的新方向。我们的研究结果有助了解肌肉再生过程中的复杂动态,对未来研发肌肉相关疾病的标靶治疗策略具有重大意义。」









