揭開RNA沉默機制的奧秘
生命科學部阮俊英教授(Tuan Anh NGUYEN)和他的團隊在分子生物學領域取得重要突破,他們的成果有望推動基因調控研究,並有助深入探索癌症、免疫系統疾病與遺傳疾病背後的機制。
Boundless:科大團隊在DICER核酸酶上有什麼最新發現?
阮教授:我們的研究帶來了重大的新發現。DICER是一種在基因沉默中起關鍵作用的酶,我們發現它其實擁有一種「雙口袋」機制,可以精確地量度RNA長度,從而決定切割的位置,猶如一把「精密剪刀」。這個發現顛覆了科學界對DICER如何與RNA鏈相互作用的傳統認知。
Boundless:什麼是「基因沉默」?
阮教授:基因沉默是指減少或抑制特定基因表現的現象。這個過程可以在細胞內自然發生,也可以通過人工手段誘導實現。基因沉默技術可用於阻止目標基因製造蛋白質,幫助科學家探索基因功能、研究疾病成因,並開發基因治療方法。
Boundless:為什麼DICER對基因調控如此重要?
阮教授:DICER在RNA干擾過程中擔當重要角色。RNA干擾是細胞利用小型RNA分子來實現基因沉默的一種機制︰DICER負責把長鏈RNA切割成微小RNA(microRNA),藉此調控基因表現,確保細胞正常運作。
Boundless:這次研究的主要突破是什麼?
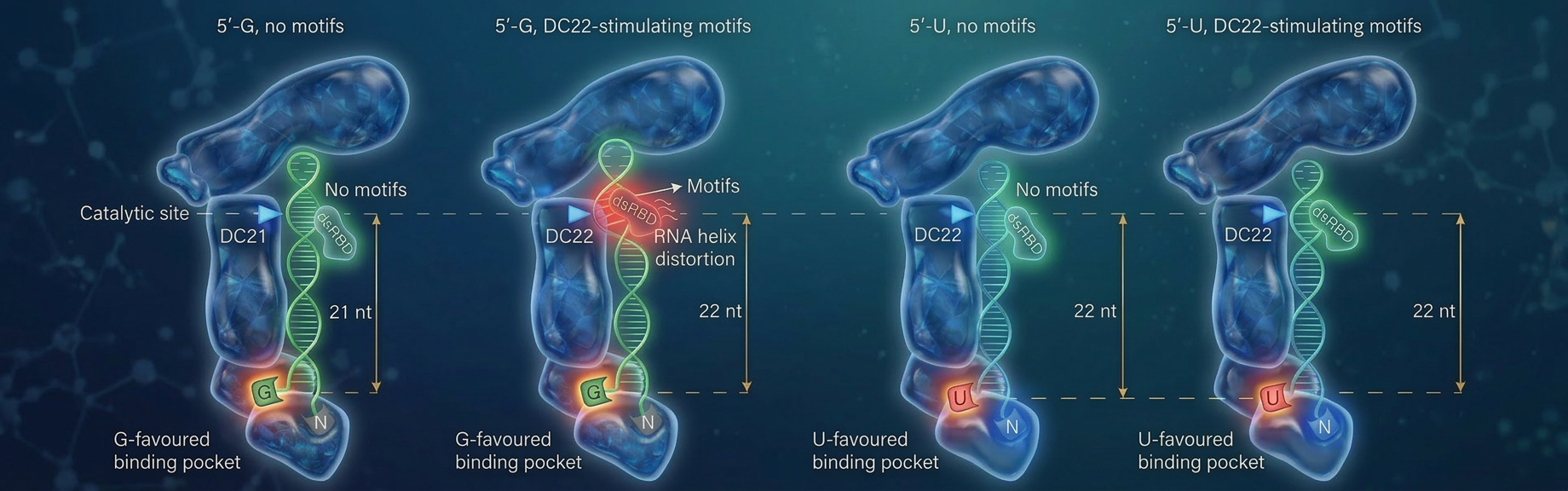
阮教授:我們首次發現了DICER中有一個「偏好辨識尿嘧啶結合口袋」(G-favored binding pocket),能夠識別以鳥嘌呤開頭的RNA鏈。在此之前,科學界以為DICER只有一種排斥鳥嘌呤的口袋。我們的新發現改寫了這個觀念,為DICER的運作機制提供了全新視角。
Boundless:研究團隊使用了哪些研究方法?
阮教授:我們結合了大數據分析與高解析度成像技術,通過大量切割實驗,觀察了數千種RNA變體與DICER互動的情形,並利用低溫電子顯微鏡(Cryo-EM)技術,在原子級別上清楚呈現DICER與RNA結合的過程。
Boundless:研究過程中遇到了哪些挑戰?
阮教授:最大的難題是如何捕捉DICER與不同RNA作用時的動態情形。過去的研究多集中在它的靜態結構,難以真正看到它的實際行為。
Boundless:研究得出的主要結論是什麼?
阮教授:簡單來說,RNA的第一個鹼基會決定它被切割的長度。若以鳥嘌呤(Guanine,G)開頭,DICER會把它剪成21個核苷酸長度;若以尿嘧啶(Uracil,U)開頭,則剪成22個核苷酸長度。這糾正了過去認為G開頭的RNA不適合被DICER切割的觀點。
Boundless:這項研究對RNA療法的未來有何意義?
阮教授: 我們必須深入理解DICER的運作方式,才能設計出高效的RNA藥物,例如常用於基因治療的shRNA。我們的研究為設計更精準鎖定基因、減少「脫靶效應」的shRNA提供了重要的基礎理論。
Boundless:下一步的研究方向是什麼?
阮教授:我們會研究DICER在面對矛盾信號時的處理機制,例如一條RNA雖然以G開頭,但其結構卻需要另一種切割長度,DICER究竟如何作出判斷?此外,我們也計劃引入人工智能與高通量方法,預測DICER與不同RNA序列的互動模式。
Boundless:此研究對分子生物學領域有什麼重大意義?
阮教授:這項研究改變了我們對microRNA生成機制的根本理解——即人體如何製造負責調控基因表現的關鍵分子。我們通過揭示DICER的精細運作,為RNA干擾療法開闢了新的可能,有望為多種疾病帶來更高效的治療方案。
Boundless:非常感謝阮教授為我們介紹這項充滿潛力的研究。此研究由阮俊英教授帶領博士生Minh Khoa NGO與Cong Truc LE共同完成,成果已發表於國際頂級期刊《自然》,論文題目為〈DICER cleavage fidelity is governed by 5’-end binding pockets〉。